De la Percepción al Placer: La Música y sus Sustratos Neuronales
Robert J. Zatorre(a), Valorie N. Salimpoor(a,b)
ABSTRACT. Music has existed in human societies since prehistory, perhaps because it allows expression and regulation of emotion and evokes pleasure. In this review, we present findings from cognitive neuroscience that bear on the question of how we get from perception of sound patterns to pleasurable responses. First, we identify some of the auditory cortical circuits that are responsible for encoding and storing tonal patterns and discuss evidence that cortical loops between auditory and frontal cortices are important for maintaining musical information in working memory and for the recognition of structural regularities in musical patterns, which then lead to expectancies. Second, we review evidence concerning the mesolimbic striatal system and its involvement in reward, motivation, and pleasure in other domains. Recent data indicate that this dopaminergic system mediates pleasure associated with music; specifically, reward value for music can be coded by activity levels in the nucleus accumbens, whose functional connectivity with auditory and frontal areas increases as a function of increasing musical reward. We propose that pleasure in music arises from interactions between cortical loops that enable predictions and expectancies to emerge from sound patterns and subcortical systems responsible for reward and valuation.
KEYWORDS. Cognition, functional imagining, auditory cortex.
Hace unos 40 000 años, una persona —un músico— recogió un hueso de buitre que tenía a todo lo largo agujeros hechos con incisiones delicadas y precisas, y le sopló para tocar una melodía. Sabemos esto gracias a los extraordinarios hallazgos arqueológicos recientes cerca del Danubio (Fig. 1) (Véase pnas.org/content/110/supplement-2/10430/F1), donde se descubrieron varias de esas flautas (Conrad, Malina y Münzel 2009). Esto lleva a la reflexión de que para que un instrumento exista en el paleolítico superior, la música debió haber existido previamente en una forma avanzada desde muchos miles de años antes; de lo contrario, habría sido imposible construir algo tan avanzado tecnológicamente como una flauta que toca una escala particular. Por lo tanto, podemos inferir con seguridad que la música se encuentra entre los rasgos cognitivos humanos más antiguos.
ORÍGENES MUSICALES
Si la música tiene orígenes antiguos es importante establecerla como parte de nuestra “maquinaria mental humana”, aunque esto no nos dice por qué pudo haberse desarrollado. La respuesta a esta pregunta puede permanecer siempre desconocida, aunque podemos consultar a Darwin para tener algún indicio. Uno de sus comentarios más conocidos sobre la música, en El origen del hombre, es el siguiente: “Como ni el placer ni la capacidad de producir notas musicales son facultades de uso inmediato para el hombre, con relación a sus hábitos ordinarios de vida, éstas deben clasificarse entre las más misteriosas con las que está dotado” [As neither the enjoyment nor the capacity of producing musical notes are faculties of the least direct use to man in reference to his ordinary habits of life, they must be ranked among the most mysterious with which he is endowed] (Darwin 1871). Diez años después, en su autobiografía, reflexionó y lamentó su propia anhedonia musical con estas palabras: “Si tuviera que vivir mi vida de nuevo, me impondría una regla para leer algo de poesía y para escuchar un poco de música, al menos una vez por semana; así, tal vez las partes de mi cerebro ahora atrofiadas se habrían mantenido activas gracias al uso. La pérdida de esos gustos es una pérdida de felicidad, y posiblemente puede que sea perjudicial para el intelecto, y más probablemente para el carácter moral, pues debilita la parte emocional de nuestra naturaleza” […if I had to live my life again, I would have made a rule to read some poetry and listen to some music at least once every week; for perhaps the parts of my brain now atrophied would thus have been kept active through use. The loss of these tastes is a loss of happiness, and may possibly be injurious to the intellect, and more probably to the moral character, by enfeebling the emotional part of our nature] (Darwin 1887). Esta reveladora observación contiene una posible respuesta al misterio aludido en la cita anterior, porque aquí Darwin formula un pensamiento con el que la mayoría de la gente intuitivamente estaría de acuerdo: que la música puede generar y potenciar emociones, y que la falta de ella da como resultado una reducción de felicidad. Incluso, él va más lejos hasta sugerir que la música puede servir para prevenir la atrofia de los circuitos neuronales asociados a la emoción, un concepto intrigante.
La mejora, la comunicación y la regulación de la emoción, sin duda constituyen razones poderosas para la existencia, y posiblemente para la evolución de la música, un tema que otros han abordado con más detalle de lo que nosotros haremos aquí (Hauser y McDermott 2003; Wallin, Merker y Brown 2000; Mithen 2005). Sin embargo, esas líneas de investigación no nos dirán por qué la música podría tener tales propiedades. La música es la más abstracta de las artes: su atractivo estético tiene poco que ver con el relato de eventos o con la representación de personas, lugares o cosas, las cuales están dentro de la competencia de las artes verbales y visuales. Una secuencia de tonos —como los que se pudieron haber producido con una flauta antigua— concatenada de una manera determinada, no puede denotar nada en particular, pero puede, sin duda, dar lugar a emociones. Los modelos psicológicos sugieren un número de mecanismos distintos asociados a las distintas respuestas emocionales que la música puede provocar (Juslin y Sloboda 2001). En el presente trabajo nos centramos específicamente en un aspecto particular de la respuesta afectiva provocada por la música: el placer. Debido a que el placer y la recompensa están relacionados y hay una vasta literatura con respecto a las bases neuronales de la recompensa, estudiar el placer musical nos da un conjunto de hipótesis que sirven de marco para estudiar lo que de otro modo podría aparecer como un tema intratable. Para entender cómo llegamos de la percepción al placer, entonces comenzamos con una visión general del análisis perceptual de los sonidos musicales, y luego pasamos a la neurobiología de la recompensa, antes de intentar una síntesis de las dos.
NEUROBIOLOGÍA DE LA COGNICIÓN MUSICAL
Al pensar en cómo la evolución pudo haber formado en particular el sistema auditivo humano, debemos considerar qué es lo más característico sobre la manera en que usamos el sonido. Un rasgo obvio que destaca es que los seres humanos utilizamos el sonido para comunicar representaciones cognitivas y estados internos, incluyendo la emoción. Ambos, el habla y la música, se pueden considerar de esta manera (Patel 2008) y uno puede ir tan lejos como decir que constituyen señales específicas de la especie [species-specific]. Por otro lado, a diferencia de los sistemas de llamado de otras especies, el nuestro es generativo y altamente recursivo, esto es, las estructuras complejas se crean de un conjunto limitado de primitivos de una manera combinatoria mediante la aplicación de reglas sintácticas. Una propiedad importante, tanto del habla como de la música, que es relevante para su naturaleza innata, es que aparecen, en la gran mayoría de los miembros de la especie, bastante temprano en el desarrollo, siguen una secuencia relativamente fija y tienen como insumo los sonidos del entorno inmediato. Por lo tanto, debe existir una arquitectura neuronal de tal manera que permita que aparezcan esas capacidades.
Tal organización neuronal necesariamente tuvo que surgir de precursores y, por ello, es útil considerar algunos de los rasgos de la corteza auditiva de los primates no humanos para identificar tanto las homologías como las propiedades únicas (Rauschecker y Scott 2009; Zatorre y Schonwiesner 2011). La corteza auditiva del primate, como el sistema visual y el sistema somatosensorial, se puede pensar organizado de manera jerárquica, tal que las áreas centrales [core] están rodeadas por las regiones cinturón [belt] y pericinturón [parabelt] dentro de la porción superior del lóbulo temporal, con los correspondientes patrones de las proyecciones de alimentación directa y de retroalimentación (Rauschecker y Scott 2009) (Fig. 2) ambos, la citoarquitectura y la conectividad de los diferentes subcampos sostienen esta organización (Kaas, Hackett y Tramo 1999). Otro rasgo de organización presente en todas las especies son las distintas trayectorias que empiezan en las áreas centrales y continúan en dos direcciones: una dorsal y posterior hacia las áreas parietales, y otra ventral y anterior dentro del lóbulo temporal (Rauschecker y Scott 2009); ambas trayectorias tienen destinos eventuales en áreas separadas de las cortezas frontales y las cuales se considera que son bidireccionales. Esta arquitectura genera una serie de bucles funcionales que permiten la integración de la información auditiva con otras modalidades; éstos también permiten interacciones entre los sistemas auditivo y motor relacionados con la acción y con la planeación u organización de la acción y con los sistemas de memoria. Esas interacciones con las funciones de planeación y de memoria dan como resultado la habilidad de hacer predicciones basadas en eventos pasados, tema al que regresaremos más adelante.
Los bucles funcionales entre las cortezas frontal y temporal también desempeñan un papel particularmente importante en la memoria de trabajo. A diferencia de los eventos visuales, que con frecuencia pueden ser estáticos (una escena, un objeto), los eventos auditivos son por su propia naturaleza efímeros, pues no dejan más rastros que aquellos que el sistema nervioso puede generar. Para ser capaz de concatenar eventos auditivos discretos, de manera tal que el significado se pueda codificar o decodificar, se necesita un sistema de memoria de trabajo que pueda mantener la información de manera dinámica para procesamientos futuros. Aquí puede residir una importante diferencia de especie: parece que los monos tienen una capacidad muy limitada para retener eventos auditivos en la memoria de trabajo (Fritz, Mishkin y Saunders 2005; Scott, Mishkin y Yin 2012) comparada con su excelente memoria de trabajo visual. Esta limitante puede ayudar a explicar la relativa escasez en su capacidad de comunicación auditiva combinatoria compleja. En contraste, los humanos tienen una excelente habilidad para mantener información auditiva conforme se va presentando, lo que representa nuestra habilidad para relacionar un sonido con otro que viene varios segundos o minutos después (considere la expresión de una larga oración cuyo significado no es claro hasta la última palabra, o una larga melodía que sólo llega a su resolución hasta el final). Varios estudios de neuroimagen han señalado las interacciones entre las cortezas auditivas y las regiones frontales inferiores, especialmente en el hemisferio derecho, en el procesamiento de la información tonal, en parte debido a las necesidades de la memoria de trabajo para las tareas tonales (Zatorre, Evans y Meyer 1994; Gaab, Gaser, Zaehle, Jancke, Schlaug 2003). De hecho, la amusia congénita o sordera de tonos (Ayotte, Peretz y Hyde 2002), se puede deber a un trastorno en este sistema (Hyde, et al. 2007; Loui, Alsop y Schlaug 2009).
La organización de mapas de frecuencia, que son en igual medida topográficos tanto en monos (Kaas y Hackett 2000; Petkov, et al. 2006) como en humanos (Formisano, et al. 2003; Schonwiesner, et al. 2002), muestran otra homología importante. Sin embargo, un rasgo más relevante para nuestra discusión es la sensibilidad a la calidad perceptual del tono. El tono es resultado de la periodicidad; tales sonidos tienen relevancia biológica debido a que por naturaleza son producidos casi exclusivamente por el tracto vocal de otros animales, en comparación con los sonidos naturales aperiódicos (aire, agua). La habilidad para seguir el tono, por lo tanto, sería un rasgo útil de un organismo para desarrollar la travesía en un ambiente acústico. Estudios neurofisiológicos han identificado neuronas sensitivas de tono en monos títis (marmosets) que responden invariablemente a sonidos que tienen el mismo tono pero que varían en su composición armónica (Bendor y Wang 2005), permitiendo así que la información de tono se procese a pesar de la irrelevante variación acústica. Varias líneas de evidencia convergen para sugerir que puede existir una especialización neuronal similar para el tono en la corteza auditiva humana, en una o más regiones localizadas a los lados de las áreas centrales (Penagos 2004; Zatorre 1988; Patterson 2002).
Con todo, en los humanos, el tono también atiende una importante función de soporte de información porque sirve como medio para codificar y transmitir información. Tanto el habla como la música hacen uso de la variación de tono, pero en la música su uso parece tener algunas propiedades particulares que lo distingue del uso en el habla (Zatorre y Baum 2012). Cabe destacar que el tono, tal como se usa en la música, en muchas culturas tiende a organizarse como elementos discretos, o escalas (a diferencia del tono en el habla donde los cambios tienden a ser continuos), y estos elementos en general tienen asociadas proporciones de frecuencia fijos y específicos. Esas propiedades son precisamente las que produciría un instrumento como nuestra flauta antigua, con los orificios fijos para los dedos que producen tonos discretos en tonos específicos. De este modo, la música requiere de un sistema nervioso capaz de codificar y producir variación de tono con un alto grado de precisión. La evidencia sustancial implica, el hemisferio cerebral derecho incluyendo las áreas corticales especializadas para el tono, a un mecanismo refinado para el tono preciso, tanto en la percepción (Zatorre y Gandour 2008; Zatorre et al. 2002; Hyde 2008) como en la producción (Ozdemir 2006), en contraste con el sistema cortical auditivo izquierdo, el cual más bien parece estar especializado en sonidos de habla que no requieren de una gran precisión en el seguimiento del tono.
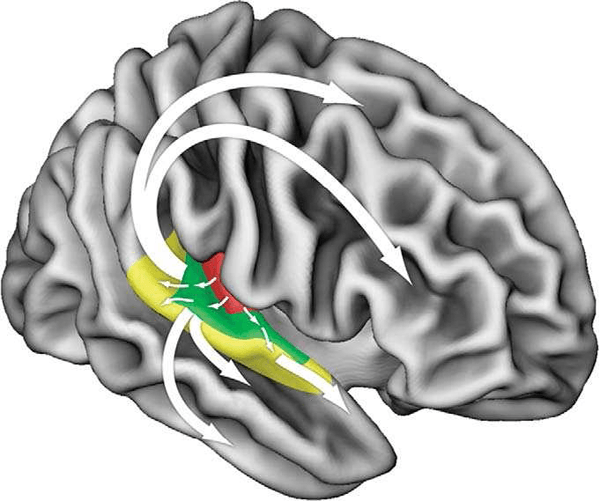
Las melodías se componen de una combinación de tonos individuales, de modo que, una vez que este primer sistema cortical codifica los tonos por separado, se necesita procesar las combinaciones de tonos. Las melodías tonales se pueden estructurar en términos de escalas a partir de las que están construidas y de los contornos del tono. Tanto los estudios de lesiones (Stewart, et al. 2006; Zatorre 1985) como los estudios de neuroi- magen (Patterson, et al. 2002, Griffiths 1998) demuestran que las áreas corticales, más allá de las regiones relacionadas con el tono, entran en juego mientras uno va de un sonido individual a los patrones de sonidos, y que éstos involucran ambos trayectos, el anteroventral y el posterodorsal, siguiendo una organización jerárquica. La imagen global que surge es que las áreas más distales del centro y de las regiones cinturón, probablemente están involucradas en el procesamiento más allá de la extracción del tono, incluyendo las combinaciones de los elementos tonales, por ejemplo, relacionados con el análisis del tamaño del intervalo musical (Klein y Zatorre 2011) y/o el contorno melódico (Lee 2011). Sin embargo, tal vez debido a la conectividad de retroalimentación de las regiones distales de regreso al centro y a las áreas cinturón, hay también pruebas de que la información de categoría auditiva algunas veces se puede codificar de manera más distribuida (Ley, et al. 2012).
Los pasos del procesamiento perceptual recién descritos solamente aluden a los mecanismos involucrados en una escucha pasiva de una secuencia de sonidos. Sin embargo, la percepción de algo como una melodía no se lleva a cabo de manera secuencial simple. Esto implica también un componente activo, de tal manera que se generan expectativas basadas en el conocimiento implícito del oyente sobre las reglas musicales que ha adquirido por exposiciones previas a la música de esa cultura. Así, escuchar un grupo particular de tonos nos lleva a esperar ciertas continuidades particulares con más probabilidad que otras (Krumhansl 1990; Huron 2006). Este fenómeno es relevante porque apunta hacia nuestra habilidad altamente adaptativa para predecir eventos futuros basados en regularidades pasadas. Existe suficiente evidencia acerca de que las contingencias secuenciales relevantes se codifican con base en un proceso de aprendizaje estadístico (Schön y Francois 2011), que emerge en una etapa temprana de la vida, tanto para el habla como para la música (Saffran 2003) y que también opera en la edad adulta (Loui 2009). Esta dependencia en la exposición al medio ambiente significa asimismo que individuos distintos tendrán grupos distintos de plantillas perceptuales en la medida en que han estado expuestos a diferentes sistemas musicales o culturales, un punto al que regresaremos más adelante.
Los sustratos neuronales asociados con las expectativas musicales y su violación se han medido utilizando marcadores electrofisiológicos. Estos estudios muestran que hay sensibilidad a las predicciones basada en una variedad de rasgos, incluyendo el contorno (Tervaniemi, et al. 2001), el tamaño del intervalo (Trainor, et al. 2002), así como las armonías (Koelsch, et al. 2000; Leino 2007). La localización de estos procesos es compleja y no del todo descifrada, pero lo más probable es que implique interacciones entre las cortezas auditivas cinturón/pericinturón y las cortezas frontales inferiores, utilizando el trayecto anteroventral antes descrito (Opitz, et al. 2002; Schönwiesner, et al. 2007). Al mantener el concepto de organización jerárquica, las violaciones a rasgos más abstractos se asocian a cambios provenientes de las áreas frontales. Por ejemplo, si se introduce un acorde que por sí mismo es consonante pero no esperado, en términos de las relaciones armónicas establecidas por acordes previos, habrá una respuesta en la corteza frontal inferior típicamente más fuerte en el lado derecho (Maess, et al. 2001; Tillmann, et al. 2006).
Desde luego, las melodías contienen patrones de tiempo así como patrones de tono. La ciencia cognitiva ha identificado cierta organización jerárquica relevante en la manera en que se procesan los ritmos (Patel 2008; Large y Palmer 2002), de tal manera que hay niveles más locales y niveles más globales. La métrica, que se define como la repetición de acentos que estructura eventos temporales, sería un nivel clave de la organización global. Ésta toma importancia en nuestro contexto porque se puede pensar como la proveedora de un marco temporal para los eventos esperados. Es decir, en la música métricamente organizada, un oyente desarrolla predicciones sobre cuándo espera que ocurran los sonidos (un paralelo de la forma en cómo la tonalidad ofrece al oyente una estructura para hacer predicciones sobre qué tonos esperar). Los estudios de neuroimagen sugieren que este mecanismo métrico puede depender de las interacciones entre las cortezas auditivas y las trayectorias más dorsales del sistema, en particular con la corteza premotora y las regiones frontales dorsolaterales (para una revisión, véase Zatorre, et al. 2007), aunque las estructuras de los ganglios basales subcorticales también juegan un papel importante (Grahn y Rowe 2009; Kung, et al. 2013). La interacción con las áreas motoras relacionadas ofrece una posible explicación de la estrecha relación entre la estructura temporal en la música y en el movimiento. No es descabellado suponer que la gente que escuchaba la música procedente de la flauta antigua también bailara.
Los hallazgos de estas líneas de investigación apuntan a la conclusión de que las interacciones entre la corteza auditiva y la corteza frontal, a lo largo de ambas trayectorias, ventral y dorsal, generan las representaciones de las regularidades estructurales de la música, que son esenciales para crear las expectativas sobre los eventos conforme se desarrollan en el tiempo. Sin duda, este sistema juega un papel clave en muchos aspectos de la percepción. De hecho, se ha descrito un fenómeno similar con relación a las expectativas lingüísticas (Friederici 2003; Patel 2003). Por otro lado, como veremos más adelante, estos mismos sistemas pueden contener parte de la clave para entender porqué la música puede provocar placer.
Un último fenómeno importante al considerar el papel de la corteza auditiva en procesos perceptuales complejos es que también participa en la imaginería, esto es, la experiencia fenomenológica de la percepción en ausencia de un estímulo. La imaginería musical es una forma particularmente relevante de esa experiencia, ya que casi cualquiera puede imaginar una pieza musical “con el oído de la mente”. La psicología cognitiva ha mostrado que las experiencias imaginarias son psicológicamente reales en la medida en que se pueden cuantificar y porque comparten rasgos de la percepción real, incluyendo precisión temporal y agudeza de tono (Halpern 1988; Janata 2012). Varios estudios de neuroimagen han mostrado la realidad neuronal de este fenómeno en tanto que incluso en ausencia de sonido, las regiones cinturón y pericinturón de la corteza auditiva son reclutadas [are recruited] de manera consistente cuando las personas realizan tareas específicas de imaginación (Zatorre y Halpern 2005, Herholz 2008). Esta habilidad de imaginar es relevante en este caso porque muestra que la corteza auditiva debe contener rastros de la memoria de eventos perceptuales pasados, y que esos rastros no son sólo de naturaleza semántica, sino más bien reflejan atributos perceptuales del sonido que originalmente se experimentaron. En el caso de la música, podemos decir que esos rastros, acumulados en el tiempo, también se pueden considerar como plantillas que contienen información sobre los patrones de sonido que se repiten en las estructuras musicales. Si esa información está almacenada en las áreas corticales, uno se podría preguntar cómo se recupera o se accede a esa información. Aunque el mecanismo está lejos de ser comprendido, parece que los bucles frontotemporales, mencionados anteriormente, son relevantes para la recuperación. Esta conclusión se apoya en la evidencia de que las interacciones funcionales entre la corteza temporal y la corteza frontal mejoran durante la imaginería musical (Herholz 2012). Es más, el grado de actividad en esta red sirve como factor de predicción para las diferencias individuales en cuanto a la intensidad subjetiva de la imaginería, lo que apoya la relación directa entre la participación de este sistema frontotemporal y la habilidad para imaginar música. Esta red, como veremos, también puede jugar un papel importante en el placer mediado por la música y en el reclutamiento [the recruitment] de la red de recompensa, tema que abordaremos ahora.
NEUROBIOLOGÍA DE LA RECOMPENSA
Una recompensa se puede pensar como algo que produce una sensación hedónica de placer. Debido a que este es un estado positivo, tendemos a reforzarlo al repetir el comportamiento que nos lleva a ese resultado deseable (Thorndike 1911). Un sustrato biológico para el refuerzo se descubrió en Montreal hace más de medio siglo, cuando Olds y Milner (1954) informaron que un estímulo eléctrico en una parte específica del cerebro de un ratón provocaba que el animal regresara de manera continua al lugar donde se realizaba el estímulo. Estudios posteriores demostraron que si a las ratas se les daba la oportunidad de estimular esas áreas, renunciaban a todas las otras conductas rutinarias, como asearse, comer y dormir (Wise 1978; Routtenberg y Lindt 1965). La estimulación eléctrica estaba dirigida a los trayectos que conducen al estrato mesolímbico, y ahora se ha demostrado ampliamente que la liberación de dopamina en esas regiones puede dar lugar al refuerzo de las conductas (Schultz 2007; Leyton 2010; Glimcher 2011).
En el reino animal, el sistema mesolímbico de recompensa filogenética- mente antiguo sirve para reforzar conductas biológicamente importantes, como comer (Hernández y Hoebel 1988), reproducirse (Pfaus, et al. 1995) o cuidar a los hijos (Hansen, et al. 1993). En los humanos, también se ha demostrado que la liberación de dopamina y la actividad hemodinámica en las áreas mesolímbicas refuerzan las conductas biológicamente adaptativas, como comer (Small, et al. 2003) y aquellas relacionadas con el amor y el sexo (Ron, et al. 2005; Komisaruk y Whipple 2005). Sin embargo, conforme los animales se hacen más complejos, otros factores adicionales se vuelven importantes para la supervivencia exitosa. Por ejemplo, entre las sociedades humanas, al tener cierta cantidad de dinero se puede predecir una supervivencia exitosa. No sorprende que obtener dinero sea altamente reforzador, y se ha demostrado que involucra a las áreas meso- límbicas estratales (Knutson, et al. 2001). Las cualidades del refuerzo de tales recompensas secundarias sugieren que los humanos son capaces de entender el valor conceptual de un elemento abstracto que no contiene valor de recompensa inmediato. En línea con esto, muchas personas obtienen placer de otros estímulos que conceptualmente tienen sentido, con poca relevancia directa para la supervivencia, y un ejemplo es escuchar música. Como mencionó Darwin, la música no tiene ninguna consecuencia funcional fácilmente evidente y ninguna función adaptativa bien definida (Hauser y McSermott 2003). No obstante, escuchar música es una actividad omnipresente en todas las sociedades humanas, por lo menos desde el paleolítico. ¿De qué manera una secuencia de sonidos, en apariencia abstracta, genera esos efectos potentes y de refuerzo?
¿CÓMO CAUSA LA MÚSICA PLACER?
Se cree en general que el placer que las personas experimentan con la música se relaciona con las emociones inducidas por la música, como lo reportan con frecuencia quienes escuchan música para cambiar o mejorar sus emociones (Juslin y Sloboda 2001). Para analizar esta relación, realizamos un experimento en el que le pedimos a los oyentes que seleccionaran música muy agradable y que mientras la escuchaban evaluaran constantemente su experiencia de placer, mientras tanto nosotros registramos cualquier cambio en la excitación emocional (Salimpoor, et al. 2009). El incremento en la actividad del sistema nervioso simpático está relacionado con las respuestas de “lucha o fuga” (fight or flight) (Cacioppo, et al. 2007) y se cree que son automatizadas; por esta razón, sirven como medida confiable de la excitación emocional. Medimos la frecuencia cardiaca, la frecuencia respiratoria, la conductividad de la piel, la temperatura corporal y la amplitud del volumen sanguíneo del pulso para rastrear los cambios que corresponden al aumento en los niveles de placer autorre- portado. Los resultados revelaron una fuerte correlación positiva entre la evaluación del placer en vivo y los incrementos registrados al mismo tiempo durante la actividad del sistema nervioso simpático, mostrando así una relación entre los índices objetivos de la excitación y los sentimientos subjetivos de placer.
![FIGURA 3. Correlatos neuronales del procesamiento de la música altamente recompensante. (A) Análisis de conjunción espacial entre [11C] tomografía de emisión de positrones raclopride y fMRI mientras los oyentes escuchan la música placentera que eligieron reveló aumento de la actividad hemodinámica en el estrato ventral (EV) durante los momentos emotivos pico (marcados por "escalofríos") y el estrato dorsal (ED) previo a los escalofríos, en las mismas regiones que mostraron liberación de dopamina. Adaptado de Komisaruk y Whipple 2005. (B) La imagen del escaneo de la RMf muestra que el mejor indicador del valor de recompensa de la música nueva (desconocida) (marcado por las ofertas monetarias a manera de subasta) fue la actividad en el cuerpo estriado, de manera particular en el NAcc; el NAcc también mostró un aumento de la conectividad funcional con el giro temporal superior (GTS) y el giro frontal inferior derecho (GFI) mientras el estímulo musical obtiene el valor de recompensa. Adaptado de Northcutt y Kaas 1995.](http://www.centrolombardo.edu.mx/wp-content/uploads/2014/10/40-15_zatorre_salimpoor-2.png)
Posteriormente, nos ocupamos de los mecanismos a través de los cuales la excitación emocional se puede volver recompensante. Si las respuestas emocionales a la música están dirigidas hacia la actividad dopaminérgica en los circuitos reforzadores del cerebro, debería haber un mecanismo con el que esas respuestas se puedan considerar recompensantes. Para analizar este punto, nuestro laboratorio realizó dos estudios en los que los participantes eligieron la música que consideraban muy emotiva y placentera (Blood y Zatorre 2001; Salimpoor, et al. 2011). Para tener una medida objetiva de la excitación emocional pico, las personas trajeron música que les causa escalofríos, los cuales se cree que son la manifestación física de las respuestas emocionales pico (Blood y Zatorre 2001; Panksepp 1995; Rickard 2004) y que están relacionados con el aumento de la excitación del sistema nervioso simpático. En el primer estudio, demostramos que el estrato ventral y otras regiones del cerebro asociados con la emoción se reclutaron como una función del aumento de la intensidad de la respuesta de escalofríos (Blood y Zatorre 2001). Este hallazgo identificó de manera importante que el sistema mesolímbico de recompensa se puede activar por un estímulo estético abstracto. Otros estudios han mostrado hallazgos consistentes (Koelsch, et al. 2006; Menon y Levitin 2005); sin embargo, dado que todos esos estudios midieron las respuestas hemodinámicas, no abordaron si el sistema dopaminérgico estaba involucrado. Realizamos entonces otro estudio (Fig. 3A) con tomografía de emisión de positrones (TEP) basado en ligadura (Salimpoor, et al. 2011), usando raclopride, un ligador de radio que se fija de manera competitiva con los receptores de dopamina. Comparamos la liberación de dopamina en la respuesta a la música placentera vs. la música neutral, y confirmamos que las respuestas emocionales fuertes a la música dan lugar a la liberación de dopamina en el estrato mesolímbico, lo que puede ayudar a explicar por qué se considera a la música como recompensante, y por qué se relaciona la música directamente con el otro estímulo biológicamente recompensante que se describió arriba.
Si los placeres asociados con la música son al menos en parte relacionados con los sistemas dopaminérgicos que compartimos con muchos otros vertebrados, ¿por qué parece que son únicamente parte de la conducta humana? ¿Pueden los animales diferenciar entre flautas antiguas, Mahler y Britney Spears? Y si así fuera, ¿les importa? El fenómeno más cercano a la música en el reino animal son las vocalizaciones biológicamente significativas. Sin embargo, se cree que esos sonidos musicales se limitan a un papel de adaptación hacia la defensa del territorio y a la atracción de la pareja, más que a un placer abstracto (Catchpole y Slater 1995; Marler 1999). Cuando a nuestros parientes evolutivos cercanos (tamarines y titíes), se les da a elegir entre escuchar música o el silencio, en general prefieren el silencio (McDermott y Hauser 2007). Algunos animales pueden ser capaces de procesar aspectos básicos del sonido de importancia para la música. Por ejemplo, los monos rhesus sí demuestran una habilidad para juzgar que dos melodías son la misma cuando se transportan una o dos octavas (Wright, et al. 2000). No obstante, esta habilidad es limitada: los monos fallaron en esta tarea si la melodía se transportaba media o una y media octava. También hay algo de evidencia (Fishman, et al. 2001; Izumi 200) acerca de que los monos pueden distinguir entre consonancias y disonancias. Sin embargo, no parece que consideran los sonidos consonantes como más placenteros, basados en los hallazgos (McDermott y Hauser 2004) sobre los monos tamarinos cabeza de algodón quienes mostraron una clara preferencia por los chillidos de alimentación específicos de la especie sobre los llamados de auxilio, aunque ninguna preferencia por intervalos consonantes vs. intervalos disonantes. Aun cuando ciertos individuos de algunas especies demuestran entrenamiento motor a estímulos rítmicos generados de manera externa (Schachner, et al. 2009; Patel, et al. 2009), no hay evidencia de que los primates hagan eso; es más, tales conductas se han observado en interacciones con los humanos y no en ambientes naturales. Así, después de todo, hay escasa evidencia de que otras especies tengan la maquinaria mental para decodificar la música de la manera en que los humanos lo hacen, o para disfrutar de ella.
¿Por qué ciertas combinaciones de sonidos parecen estéticamente agradables para los humanos pero no para otros animales, incluso primates? Para entender mejor cómo podemos recibir placer de los sonidos musicales, es importante darnos cuenta de que los sistemas mesolímbicos no trabajan de manera aislada y que su influencia dependerá en gran medida de su interacción con otras regiones del cerebro. Las regiones mesolímbicas estratales se encuentran en muchos organismos, incluyendo los primeros vertebrados (O’Connell y Hofmann 2011); no obstante la conectividad anatómica de estas regiones con el resto del cerebro varía entre las especies dependiendo de la complejidad del cerebro (Northcutt y Kaas 1995). Por ejemplo, el sistema mesolímbico de recompensa se vuelve altamente interconectado con las cortezas prefrontales en los mamíferos (Cardinal, et al. 2005). Más aún, conforme los animales se vuelven más complejos, el concepto de recompensa puede tomar distintas formas. Por ejemplo, nosotros los humanos disfrutamos de actividades tan diversas como ir a conciertos, leer ficción, visitar museos, o tomar fotografías, así como de actividades menos “intelectuales”, aunque estéticas, como decorar nuestros vehículos, combinar nuestra vestimenta o plantar flores. Las recompensas estéticas son con frecuencia de naturaleza abstracta y en general implican componentes cognitivos importantes. En particular, dependen en gran medida de la cultura y por ello implican un papel crítico en el aprendizaje y en las influencias sociales. Estas características sugieren que pueden involucrar a regiones del cerebro de “orden superior” que están más evolucionadas en los humanos. Los estudios de imagen cerebral del procesamiento de recompensa estética apoyan esta idea al demostrar actividad en la corteza cerebral, particularmente en la corteza prefrontal (Vartanian y Goel 2004; Kawabata y Zeki 2004; Cela-Conde et al. 2004), que es la más evolucionada en los humanos (Haber y Knutson 2010). La corteza cerebral contiene almacenes de información acumulada a lo largo de la existencia de un organismo. Es así como las contribuciones corticales al procesamiento de estímulos estéticos son consistentes con la idea de que las experiencias previas pueden jugar un papel fundamental en la manera en la que un individuo puede experimentar ciertos sonidos como agradables o recompensantes. Aunque existe evidencia sobre algunas similitudes básicas en cómo las personas de todas las culturas responde a ciertas señales (Fritz, et al. 2009), la naturaleza de la recompensa a estímulos estéticos no es del todo universal, pues difiere de manera significativa entre las culturas y entre los individuos dentro de cada cultura. Esas respuestas se relacionan con la interpretación subjetiva del estímulo, que es probable que esté relacionado a experiencias previas con un estímulo en particular u otro estímulo similar. Se ha propuesto que los individuos tienen un “léxico musical” (Peretz y Coltheart 2003), que representa un sistema de almacenaje para la información musical a la cual se han expuesto durante su vida, incluyendo la información sobre las relaciones entre los sonidos y las reglas sintácticas de la estructura específica de la música de sus experiencias previas. Este sistema de almacenaje puede contener plantillas que se pueden aplicar a la información entrante de sonido para ayudar a la persona a clasificar y entender mejor qué es lo que él o ella está escuchando. Así, cada vez que se escucha una secuencia de sonidos, se pueden activar varias plantillas para ajustarse a la información auditiva entrante. Este proceso conducirá inevitablemente a una serie de predicciones que pueden confirmarse o violarse, y determinar finalmente el valor de recompensa para el individuo.
Para analizar los sustratos neuronales de las predicciones y la recompensa asociados con la música, y cómo éstos pueden contribuir a las respuestas de placer, en un nuevo estudio escaneamos a personas con resonancia magnética funcional (RMf) mientras escuchaban música que no habían oído antes y examinamos la actividad neuronal asociada con el valor de recompensa de la música (Salimpoor, et al. 2013). Examinamos el valor de recompensa de cada pieza musical, dándole a las personas la oportunidad de comprarlas a manera de subasta (Becker et al. 1964); así las ofertas monetarias más altas nos sirvieron como indicadores de los valores de recompensa más altos. Estábamos interesados en analizar la actividad neuronal asociada a la escucha por primera vez de secuencias musicales y en analizar la actividad neuronal que puede distinguir entre secuencias musicales que se convierten en “recompensa” para un individuo, en comparación con aquellas que no les importaba escuchar de nuevo. Los resultados (Fig. 3B) revelaron que la actividad en las áreas mesolímbicas estratales, en particular el núcleo accumbens (NAcc), fue el que más se asoció con el valor de recompensa del estímulo musical, tal como se midió por el monto de la oferta. El NAcc se ha relacionado con las predicciones, con las anticipaciones y con la recompensa de la predicción de errores -esto es, la diferencia calculada entre lo que se esperaba y el resultado real (O’Doherty 2004, Pessiglione, et al. 2006; McClure 2003). Una predicción puede resultar en una predicción positiva, en una predicción cero o en una predicción negativa, dependiendo de las expectativas del organismo y del resultado (Sutton y Barto 1998; Schultz 1998; Montague 1996), y diversos estudios han demostrado que la predicción de errores está relacionada con las neuronas de dopamina en el mesencéfalo (Bayer y Glimcher 2005; Morris et al. 2004) y que se pueden medir en el NAcc (O’Doherty 2004, Pessiglione et al. 2006). Por lo tanto, este resultado ofrece evidencia de que las predicciones temporales juegan un papel importante en la manera en que las personas obtienen placer del estímulo musical. Un segundo hallazgo, y quizás más importante, fue que las cortezas auditivas en el giro temporal superior (GTS), que estaban alta e igualmente activas durante todo el procesamiento del estímulo musical, mostraron un fuerte incremento de las interacciones funcionales con el NAcc durante el procesamiento de las secuencias musicales con valor de recompensa alta, en comparación con las de valor de recompensa bajo. Como se argumentó arriba, las cortezas auditivas son los sitios donde se procesa no solamente la información auditiva entrante, sino también donde se procesan los cálculos más abstractos relacionados con la percepción, la imaginería y la predicción temporal. El incremento de la conectividad funcional entre el NAcc y el GTS conforme aumenta el valor de recompensa sugiere que las predicciones estaban relacionadas con la información contenida en el GTS, el cual, pensamos, está relacionado con las plantillas de información de sonido reunidas a través de las experiencias previas de la persona con los sonidos musicales (probablemente en parte basado en el conocimiento implícito, como podría surgir a través del aprendizaje estadístico). Esta interacción funcional entre los circuitos subcorticales de recompensa implicados en la predicción y las regiones altamente individualizadas de la corteza cerebral pueden explicar por qué a distintas personas les gusta música distinta, y cómo esto puede ser una función de sus experiencias previas con los sonidos musicales. Es más, en consonancia con los estudios revisados anteriormente que relacionan el GTS con la corteza frontal inferior y que implica a esta región con las expectativas jerárquicas durante el procesamiento de la música, encontramos también un aumento en la conectividad de la corteza frontal con el NAcc durante el procesamiento de la música altamente recompensante. Estas interacciones corticoestratales son ejemplo de la naturaleza cognitiva de las respuestas recompensantes a la música y ayudan a explicar porqué las complejidades del cerebro humano altamente evolucionado hacen posible la experiencia del placer a partir de la secuencia abstracta de los patrones de sonido.
En el experimento que describimos, usamos música nueva para descartar expectativas verdaderas (Bharucha 1994 ), o expectativas explícitas sobre cómo se podrían desarrollar los pasajes musicales basándose en la familiaridad con las selecciones musicales. No obstante, las expectativas explícitas también pueden llevar a la actividad en las regiones mesolímbicas estratales. En el estudio anterior (Salimpoor, et al. 2011), encontramos actividad en el estrato dorsal (núcleo caudado) durante el periodo inmediatamente anterior a los escalofríos, es decir, durante una fase de anticipación (Fig. 3A). De hecho, este componente dorsal del estrato mesolímbico se ha asociado previamente con la anticipación (Boileau, et al. 2006). El estrato dorsal tiene conexiones anatómicas intrincadas con varias zonas de la corteza prefrontal (Postuma y Dagher 2006; Monchi, et al. 2006). Los lóbulos frontales, en particular las cortezas prefrontales, están involucrados con las funciones ejecutivas, como el mantenimiento temporal de la información en la memoria de trabajo y de relacionar la información con eventos previos, establecer secuencias temporales, la planeación adelantada, la creación de expectativas, la anticipación de resultados y la planea- ción de acciones para obtener recompensas (Petrides y Pandya 2004; Stuss y Knight 2002). Estos procesos cognitivos son muy importantes durante el procesamiento musical, y sería coherente que los circuitos del cuerpo estriado ofrecieran un mecanismo de matices de tiempo que diera origen a los sentimientos de anticipación y deseo. Por ello es probable que la corteza cerebral y el cuerpo estriado trabajen juntos para hacer predicciones sobre eventos futuros potencialmente recompensantes y evalúen el resultado de esas predicciones. El apoyo adicional, que involucra al núcleo caudado en la anticipación, proviene de otros estudios que implican al estrato dorsal en la anticipación del estímulo deseable, cuando la conducta es habitual y esperada (Boileau, et al. 2006; Belin y Everitt 200 De esta manera, las señales que predicen el inicio de un evento deseado se pueden volver reforzadoras en sí. En el caso de la música, esta predicción puede incluir secuencias de sonidos que señalen el inicio de una parte de la música altamente deseada. De manera previa, los estímulos neutrales pueden volverse así condicionados para servir como pistas que señalen el inicio de la secuencia recompensante. Las cortezas frontales (Tillmann, et al. 2003; Koelsch, et al. 2008) y sus interacciones con el ganglio basal (Seger, et al. 2013) también están implicados en el procesamiento sintáctico de eventos no esperados durante la música, lo que sugiere que pueden estar involucrados en el seguimiento del desarrollo temporal de los patrones de sonido y sus relaciones estructurales, lo que apoya aún más el papel de la conectividad del cuerpo estriado con las regiones más evolucionadas del cerebro humano durante el procesamiento de la música. Es importante destacar que se ha demostrado que el NAcc también juega un papel en la anticipación con otros tipos de estímulos, tal como las recompensas monetarias (Knutson y Cooper 2005). Los papeles funcionales de estas estructuras, por lo tanto, no se atribuyen de manera simple a cualquier dimensión, sino que se modifican dinámicamente como una función de una variedad de factores, de los cuales no todos han sido aún identificados.
El NAcc jugó un papel importante tanto en la música nueva como en la conocida. En el caso de la música conocida, la actividad hemodinámica en el NAcc se asoció con el aumento de placer y su expresión máxima durante los escalofríos, lo que representa la respuesta emocional pico, y éstas fueron las mismas regiones que mostraron liberación de dopamina. El NAcc está estrechamente conectado con las áreas límbicas subcorticales del cerebro, involucradas en el procesamiento, detección y expresión de emociones, incluyendo la amígdala y el hipocampo. También está conectado al hipotálamo, la ínsula y la corteza cingulada anterior (Haber y Knutson 2010), todos implicados en el control del sistema nervioso autónomo, y tal vez responsables del fenómeno psicofisiológico asociado con el escuchar música y la excitación emocional. Finalmente, el NAcc está íntimamente integrado con las áreas corticales involucradas en el procesamiento de “alto nivel” de las emociones que integran información de varias fuentes, incluyendo el orbital y el lóbulo frontal ventromedial. Estas áreas están extensamente involucradas en la asignación y el mantenimiento del valor de recompensa del estímulo (O’Doherty 2004; Chib, et al. 2009) y pueden ser críticas en la evaluación de la prominencia del estímulo abstracto que consideramos placentero.
PONIENDO TODO JUNTO
Los estudios que hemos revisado comienzan a señalar el camino hacia una comprensión neurobiológica de cómo los patrones de sonido, de algún modo sin sentido, pueden dar lugar a experiencias placenteras altamente recompensantes. Los conceptos clave giran entorno a la idea de las expectativas temporales, a sus predicciones asociadas y al valor de recompensa generado por esas predicciones. Como hemos visto, las regiones corticales auditivas contienen especializaciones para el análisis y la codificación de los atributos básicos del sonido que están presentes en la música, en particular los valores de tono y duración. Estos elementos se procesan de manera jerárquica dentro de las áreas auditivas para representar patrones de sonido en oposición a los sonidos individuales. Las interacciones entre las áreas auditivas y las cortezas frontales a través de las rutas ventral y dorsal son críticas al permitir a la memoria de trabajo tejer los sonidos separados en representaciones más abstractas, y a su vez, generar expectativas tonales y temporales sobre la base de regularidades estructurales encontradas en la música. Esas expectativas están enraizadas en templetes derivados de la historia de escucha del individuo, que se almacena probablemente en la corteza auditiva.
El sistema de recompensa, filogenéticamente antiguo, se puede explicar con más parsimonia como un mecanismo que promueve ciertas conductas adaptativas, con circuitos dopaminérgicos que juegan un papel fundamental en el establecimiento de la prominencia y el valor de recompensa de estímulos relevantes y las sensaciones generadas por ellos. Una parte importante de este sistema parece que se dedica a premiar la predicción; como se indicó antes, el cumplimiento de las predicciones lleva a la liberación de dopamina en el cuerpo estriado, con una mayor respuesta asociada a la recompensa mejor que la esperada. Los hallazgos de las interacciones funcionales mejoradas entre las cortezas auditivas, las cortezas relacionadas con la evaluación y el cuerpo estriado como una función de cuánto una nueva pieza musical pueda gustar, ofrece una liga entre esas dos grandes líneas de investigación. Sugerimos que las interacciones que observamos representan un diálogo simultáneo y aumentado de información entre los sistemas responsables del análisis de patrones y de predicción (cortical) con los sistemas responsables de la asignación del valor de recompensa mismo (subcortical). Por lo tanto, el sistema cortical altamente evolucionado es capaz de decodificar las relaciones tonales o rítmicas, en niveles de organización tanto locales como globales, que se encuentran en la música, de tal manera que puede generar expectativas sobre eventos futuros en función de eventos pasados. Sin embargo, la excitación emocional asociada con esos patrones, pensamos, se genera por las interacciones con el sistema dopaminérgico estriado. Este marco, y otros similares (Kringelbach y Vuust 2009), también se puede considerar más amplio en tanto que se puede aplicar a otro tipo de recompensas estéticas: por ejemplo, algunos autores han sugerido que las experiencias visuales estéticas pueden surgir de las interacciones entre las regiones corticales involucradas en la percepción y en la memoria (Biederman y Vessel 2006); de modo similar, Cela-Conde et al. (2013), enfatizan la sincronización de los campos corticales tan importantes para la estética visual.
Nuestra habilidad para disfrutar de la música quizás se puede ver ahora un poco menos misteriosa de lo que Darwin pensaba, cuando la vio como el resultado de la maquinaria humana mental; vemos su antigüedad filogenética, los circuitos orientados a la supervivencia, sus bucles corticales más recientemente evolucionados que nos permiten representar información, imaginar resultados, hacer predicciones y actuar conforme a nuestro conocimiento acumulado. Tenemos pocas dudas de que los antiguos músicos, armados con la misma maquinaria que nosotros y capaces de coaccionar los patrones tonales de un hueso de buitre, experimentaron y comunicaron placer, belleza y asombro tal y como lo hacemos ahora.
Traducción de Lucía González.
a) Montreal Neurological Institute, McGill University, Montreal, QC, Canada H3A 2B4; b) Rotman Research Institute, Baycrest Centre, University of Toronto, Toronto, ON, Canada M6A 2E1. / robert.zatorre@mcgill.ca / RJZ y VNS escribieron el artículo.
Ludus Vitalis, vol. XXI, num. 40, 2013, pp. 293-317.
REFERENCIAS
Aron, A., et al. (2005), “Reward, motivation, and emotion systems associated with earlystage intense romantic love”, J. Neurophysiol 94(1): 327-337.
Ayotte, J., I. Peretz y K. Hyde (2002), “Congenital amusia: A group study of adults aflicted with a music-specific disorder”, Brain 125(Pt 2): 238-251.
Bayer, H. M. y P. W. Glimcher (2005), “Midbrain dopamine neurons encode a quantitative reward prediction error signal”, Neuron 47(1): 129-141.
Becker, G. M., M. H. DeGroot y J. Marschak (1964), “Measuring utility by a single-response sequential method”, Behav Sci 9(3): 226-232.
Belin, D. y B. J. Everitt (2008), “Cocaine seeking habits depend upon dopamine- dependent serial connectivity linking the ventral with the dorsal striatum”, Neuron 57(3): 432-441.
Bendor D. y X. Wang (2005), “The neuronal representation of pitch in primate auditory cortex”, Nature 436(7054): 1161-1165.
Bharucha, J. (1994), Tonality and Expectation. Musical Perceptions. R. Aiello (ed.). Oxford: Oxford University Press, pp. 213-239.
Biederman, I. y E. Vessel (2006), “Perceptual pleasure and the brain”, Am Sci 94: 249-255.
Blood, A. J. y R. J. Zatorre (2001), “Intensely pleasurable responses to music correlate with activity in brain regions implicated in reward and emotion”, Proc Natl Acad Sci USA 98(20): 11818-11823.
Boileau, I. et al. (2006), “Modeling sensitization to stimulants in humans: An [11C] raclopride/positron emission tomography study in healthy men”, Arch Gen Psychiatry 63(12): 1386-1395.
Cacioppo, J. T., L. G. Tassinary y G. G Berntson (2007), Handbook of Psychophysiology. New York: Cambridge University Press.
Cardinal R. N., J. A. Parkinson, J. Hall y B. J. Everitt (2002), “Emotion and motivation: The role of the amygdala, ventral striatum, and prefrontal cortex”, Neurosci Biobehav Rev 26(3): 321-352.
Catchpole, C. K. y P. J. B. Slater (1995), Bird Song: Biological Themes and Variations. Cambridge: Cambridge University Press.
Cela-Conde, C. J., et al. (2004), “Activation of the prefrontal cortex in the human visual aesthetic perception”, Proc Natl Acad Sci USA 101(16): 6321-6325.
Cela-Conde, C. J. et al. (2013), “Dynamics of brain networks in the aesthetic appreciation”. Proc Natl Acad Sci USA, 10.1073/pnas. 1302855110.
Chib, V. S., A. Rangel, S. Shimojo y J. P. O’Doherty (2009), “Evidence for a common representation of decision values for dissimilar goods in human ventromedial prefrontal cortex”, J Neurosci 29(39): 12315-12320.
Conard, N. J., M. Malina y S. C. Munzel (2009), “New flutes document the earliest musical tradition in southwestern Germany”, Nature 460(7256): 737-740.
Darwin, Ch. (1871), The Descent of Man, and Selection in Relation to Sex. London: John Murray.
Darwin, Ch. (1887), The Life and Letters of Charles Darwin. London: John Murray.
Fishman Y. I. et al. (2001), “Consonance and dissonance of musical chords: Neural correlates in auditory cortex of monkeys and humans”, J Neurophysiol 86(6): 2761-2788.
Formisano, E. et al. (2003), “Mirror-symmetric tonotopic maps in human primary auditory cortex”, Neuron 40(4): 859-869.
Friederici, A. D., S-A. Ruschemeyer, A. Hahne y C. J. Fiebach (2003), “The role of left inferior frontal and superior temporal cortex in sentence comprehension: Localizing syntactic and semantic processes”, Cereb Cortex 13(2): 170-177.
Fritz J., M. Mishkin y R. C. Saunders (2005), “In search of an auditory engram”, Proc Natl Acad Sci USA 102(26): 9359-9364.
Fritz, T. et al. (2009), “Universal recognition of three basic emotions in music”, Curr Biol 19(7): 573-576.
Gaab, N., C. Gaser, T. Zaehle, L. Jancke y G. Schlaug (2003), “Functional anatomy of pitch memory—an fMRI study with sparse temporal sampling”, Neuroimage 19(4): 1417-1426.
Glimcher, P. W. (2011), “Understanding dopamine and reinforcement learning: The dopamine reward prediction error hypothesis”, Proc Natl Acad Sci USA 108(Suppl 3): 15647-15654.
Grahn, J. A. y J. B. Rowe (2009), “Feeling the beat: Premotor and striatal interactions in musicians and nonmusicians during beat perception”, J Neurosci 29(23): 7540-7548.
Grifiths, T. D., C. Buchel, R. S. J. Frackowiak y R. D. Patterson (1998), “Analysis of temporal structure in sound by the human brain”, Nat Neurosci 1(5): 422-427.
Haber, S. N. y B. Knutson (2010), “The reward circuit: Linking primate anatomy and human imaging’, Neuropsychopharmacology 35(1): 4-26.
Halpern, A. R. (1988), “Mental scanning in auditory imagery for songs”, J Exp Psychol Learn Mem Cogn 14(3): 434-443.
Hansen, S., A. H. Bergvall y S. Nyiredi (1993), “Interaction with pups enhances dopamine release in the ventral striatum of maternal rats: A microdialysis study”, Pharmacol Biochem Behav 45(3): 673-676.
Hauser, M. D. y J. McDermott (2003), “The evolution of the music faculty: A comparative perspective”, Nat Neurosci 6(7):663-668.
Herholz, S. C., A. R. Halpern y R. J. Zatorre (2012), “Neuronal correlates of perception, imagery, and memory for familiar tunes”, J Cogn Neurosci 24(6): 1382-1397.
Herholz, S. C., C. Lappe, A. Knief y C. Pantev (2008), “Neural basis of music imagery and the effect of musical expertise”, Eur J Neurosci 28(11): 2352-2360.
Hernández, L. y B. G. Hoebel (1988), “Food reward and cocaine increase extracellular dopamine in the nucleus accumbens as measured by microdialysis”, Life Sci 42(18): 1705-1712.
Huron, D. (2006), Sweet Anticipation: Music and the Psychology of Expectaction. Cambridge, M.A.: MIT Press.
Hyde, K. L., I. Peretz y R. J. Zatorre (2008), “Evidence for the role of the right auditory cortex in fine pitch resolution”, Neuropsychologia 46(2): 632-639.
Hyde, K. L. et al. (2007), “Cortical thickness in congenital amusia: When less is better than more”, J Neurosci 27(47): 13028-13032.
Izumi, A. (2000), “Japanese monkeys perceive sensory consonance of chords”, J Acoust Soc Am 108(6): 3073-3078.
Janata, P. (2012), “Acuity of mental representations of pitch”, Ann N Y Acad Sci 1252(1): 214-221.
Juslin, P. N. y J. A. Sloboda (2001), Music and Emotion: Theory and Research. Oxford: Oxford University Press.
Kaas, J. H. y T. A. Hackett (2000), “Subdivisions of auditory cortex and processing streams in primates”, Proc Natl Acad Sci USA 97(22): 11793-11799.
Kaas, J. H., T. A. Hackett y M. J. Tramo (1999), “Auditory processing in primate cerebral cortex”, Curr Opin Neurobiol 9(2): 164-170.
Kawabata, H. y S. Zeki (2004), “Neural correlates of beauty”, J Neurophysiol 91(4): 1699-1705
Klein, M. E. y R. J. Zatorre (2011),”A role for the right superior temporal sulcus in categorical perception of musical chords”, Neuropsychologia 49(5): 878-887.
Knutson, B., C. M. Adams, G. W. Fong y D. Hommer (2001), “Anticipation of increasing monetary reward selectively recruits nucleus accumbens”, J Neurosci 21(16): RC159.
Knutson, B. y J. C. Cooper (2005), “Functional magnetic resonance imaging of reward prediction”, Curr Opin Neurol 18(4): 411-417.
Koelsch, S., T. V. Fritz, D. Y. Cramon, K. Muller y A. D. Friederici (2006), “Investigating emotion with music: An fMRI study”, Hum Brain Mapp 27(3): 239-250.
Koelsch, S., T. C. Gunter, A. D. Friederici y E. Schröger (2000), “Brain indices of music processing: “Non-musicians” are musical”, J Cogn Neurosci 12(3): 520541.
Koelsch, S., S. Kilches, N. Steinbeis y S. Schelinski (2008), “Effects of unexpected chords and of performer’s expression on brain responses and electrodermal activity”, PLoS ONE 3(7): e2631.
Komisaruk, B. R. y B. Whipple (2005), “Functional MRI of the brain during orgasm in women”, Annu Rev Sex Res 16: 62-86.
Kringelbach, M. y P. Vuust (2009), “The pleasure of music”, in Pleasures of the Brain. M. Kringelbach y K. Berridge (eds.). New York: Oxford University Press, pp. 255-269.
Krumhansl, C. L. (1990), Cognitive Foundations of Musical Pitch. New York: Oxford University Press.
Kung, S-J., J. L. Chen, R. J. Zatorre y V. B. Penhune (2013), “Interacting cortical and basal ganglia networks underlying. Finding and tapping to the musical beat”, J Cogn Neurosci 25(3): 401-420.
Large, E. W. y C. Palmer (2002), “Perceiving temporal regularity in music”, Cogn Sci 26: 1-37.
Lee, Y-S., P. Janata, C. Frost, M. Hanke y R. Granger (2011), “Investigation of melodic contour processing in the brain using multivariate pattern-based fMRI”, Neuroimage 57(1): 293-300.
Leino, S., E. Brattico, M. Tervaniemi y P. Vuust (2007), “Representation of harmony rules in the human brain: Further evidence from event-related potentials”, Brain Res 1142: 169-177.
Ley, A. et al. (2012), “Learning of new sound categories shapes neural response patterns in human auditory cortex”, J Neurosci 32(38): 13273-13280.
Leyton, M. (2010), “The neurobiology of desire: Dopamine and the regulation of mood and motivational states in humans”, in Pleasures of the Brain. M. L. Kringelbach y K. C. Berridge (eds.). New York: Oxford University Press.
Loui, P., D. Alsop y G. Schlaug (2009), “Tone deafness: A new disconnection syndrome?” J Neurosci 29(33): 10215-10220.
Loui, P., E. H. Wu, D. L. Wessel y R. T. Knight (2009), “A generalized mechanism for perception of pitch patterns”, J Neurosci 29(2): 454-459.
Maess, B., S. Koelsch, T. C. Gunter y A. D. Friederici (2001), “Musical syntax is processed in Broca’s area: An MEG study”, Nat Neurosci 4(5):540-545.
Marler, P. (1999), “Origins of music and speech: Insights from animals”, in The Origins of Music. N. L. Wallin, B. Merker y S. Brown (eds.). Cambridge, M. A.: MIT Press.
McClure, S. M., G. S. Berns y P. R. Montague (2003), “Temporal prediction errors in a passive learning task activate human striatum”, Neuron 38(2): 339-346.
McDermott, J. y M. Hauser (2004), “Are consonant intervals music to their ears? Spontaneous acoustic preferences in a non-human primate”, Cognition 94(2): B11-B21.
McDermott, J. y M. D. Hauser (2007), “Non-human primates prefer slow tempos but dislike music overall”, Cognition 104(3): 654-668.
Menon, V. y D. J. Levitin (2005), “The rewards of music listening: Response and physiological connectivity of the mesolimbic system”, Neuroimage 28(1): 175184.
Mithen, S. (2005), The Singing Neanderthals: The Origins of Music, Language, Mind and Body. London: Weidenfeld & Nicolson.
Monchi, O., M. Petrides, A. P. Strafella, K. J. Worsley y J. Doyon (2006), “Functional role of the basal ganglia in the planning and execution of actions”, Ann Neurol 59(2): 257-264.
Montague, P. R., P. Dayan y T. J. Sejnowski (1996), “A framework for mesencephalic dopamine systems based on predictive Hebbian learning”, J Neurosci 16(5): 1936-1947.
Morris, G., D. Arkadir, A. Nevet, E. Vaadia y H. Bergman (2004), “Coincident but distinct messages of midbrain dopamine and striatal tonically active neurons”, Neuron 43(1): 133-143.
Northcutt, R. G. y J. H. Kaas (1995), “The emergence and evolution of mammalian neocortex”, Trends Neurosci 18(9): 373-379.
O’Connell, L. A. y H. A. Hofmann (2011), “The vertebrate mesolimbic reward system and social behavior network: A comparative synthesis”, J Comp Neurol 519(18): 3599-3639.
O’Doherty, J. P. (2004), “Reward representations and reward-related learning in the human brain: Insights from neuroimaging’, Curr Opin Neurobiol 14(6): 769-776.
Olds, J. y P. Milner (1954), “Positive reinforcement produced by electrical stimulation of septal area and other regions of rat brain”, J Comp Physiol Psychol 47(6): 419-427.
Opitz, B., T. Rinne, A. Mecklinger, D. Y. von Cramon y E. Schroger (2002), “Differential contribution of frontal and temporal cortices to auditory change detection: fMRI and ERP results”, Neuroimage 15(1): 167-174.
Ozdemir, E., A. Norton y G. Schlaug (2006), “Shared and distinct neural correlates of singing and speaking”, Neuroimage 33(2): 628-635.
Panksepp, J. (1995), “The emotional source of “chills” induced by music”, Music Percept 13:171-207.
Patel, A. D. (2003), “Language, music, syntax and the brain”, Nat Neurosci 6(7): 674-681.
Patel, A. D., J. R. Iversen, M. R. Bregman y I. Schulz (2009), “Experimental evidence for synchronization to a musical beat in a non-human animal”, Curr Biol 19(10): 827-830.
Patel, A. D. (2008). Music, Language, and the Brain. Oxford University Press, New York.
Patterson, R. D., S. Uppenkamp, I. S. Johnsrude y T. D. Grifiths (2002), “The processing of temporal pitch and melody information in auditory cortex”, Neuron 36(4): 767-776.
Penagos, H., J. R. Melcher y A. J. Oxenham (2004), “A neural representation of pitch salience in nonprimary human auditory cortex revealed with functional magnetic resonance imaging”, J Neurosci 24(30): 6810-6815.
Peretz. I. y M. Coltheart (2003), “Modularity of music processing”, Nat Neurosci 6(7): 688-691.
Pessiglione, M., B. Seymour, G. Flandin, R. J. Dolan y C. D. Frith (2006), “Dopamine-dependent prediction errors underpin reward-seeking behaviour in humans”, Nature 442 (7106): 1042-1045.
Petkov, C. I., C. Kayser, M. Augath y N. K. Logothetis (2006), “Functional imaging reveals numerous fields in the monkey auditory cortex”, PLoS Biol 4(7): e215.
Petrides, M. y D.N. Pandya (2004), The Frontal Cortex. The Human Nervous System. G. Paxinos y J. K. Mai (eds.). 2a. ed. New York: Elsevier.
Pfaus, J. G., G. Damsma, D. Wenkstern y H. C. Fibiger (1995), “Sexual activity increases dopamine transmission in the nucleus accumbens and striatum of female rats”, Brain Res 693(1-2): 21-30.
Postuma, R. B. y A. Dagher (2006), “Basal ganglia functional connectivity based on a meta-analysis of 126 positron emission tomography and functional magnetic resonance imaging publications”, Cereb Cortex 16(10): 1508-1521.
Rauschecker, J. P. y S. K. Scott (2009), “Maps and streams in the auditory cortex: non-human primates illuminate human speech processing”, Nat Neurosci 12(6): 718-724.
Rickard, N. S. (2004), “Intense emotional responses to music: A test of the physiological arousal hypothesis”, Psychol Music 32(4): 371-388.
Routtenberg, A. y J. Lindy (1965), “Effects of the availability of rewarding septal and hypothalamic stimulation on bar pressing for food under conditions of deprivation”, Journal of Comparative and Psychophysiological Psychology 60: 158161.
Saffran, J. R. (2003), “Mechanisms of musical memory in infancy”, The Cognitive Neuroscience of Music. I. Peretz y R. J. Zatorre (eds.). New York: Oxford University Press, pp. 32-41.
Salimpoor, V. N. et al. (2013), “Interactions between the nucleus accumbens and auditory cortices predict music reward value”, Science 340(6129): 216-219.
Salimpoor, V. N., M. Benovoy, K. Larcher, A. Dagher y R. J. Zatorre (2011), “Anatomically distinct dopamine release during anticipation and experience of peak emotion to music”, Nat Neurosci 14(2): 257-262.
Salimpoor, V. N., M. Benovoy, G. Longo, J. R. Cooperstock y R. J. Zatorre (2009), “The rewarding aspects of music listening are related to degree of emotional arousal”, PLoS ONE 4(10): e7487.
Schachner, A., T. F. Brady, I. M. Pepperberg y M. D. Hauser (2009), “Spontaneous motor entrainment to music in multiple vocal mimicking species”, Curr Biol 19(10): 831-836.
Schön, D. y C. Francois (2011), “Musical expertise and statistical learning of musical and linguistic structures”, Front Psychol 2: 167.
Schönwiesner, M. et al. (2007), “Heschl’s gyrus, posterior superior temporal gyrus, and mid-ventrolateral prefrontal cortex have different roles in the detection of acoustic changes”, J Neurophysiol 97(3): 2075-2082.
Schönwiesner, M., D. Y. von Cramon y R. Rubsamen (2002), “Is it tonotopy after all?”, Neuroimage 17(3): 1144-1161.
Schultz, W. (1998), “Predictive reward signal of dopamine neurons”, J Neurophysiol 80(1): 1-27.
Schultz, W. (2007), “Behavioral dopamine signals”, Trends Neurosci 30(5): 203210.
Scott, B. H., M. Mishkin y P. Yin (2012), “Monkeys have a limited form of short-term memory in audition”, Proc Natl Acad Sci USA 109(30): 12237-12241.
Seger, C. A. et al. (2013), “Corticostriatal contributions to musical expectancy perception”, J Cogn Neurosci, 10.1162/jocn_a_00371.
Small, D. M., M. Jones-Gotman y A. Dagher (2003), “Feeding-induced dopamine release in dorsal striatum correlates with meal pleasantness ratings in healthy human volunteers”, Neuroimage 19(4): 1709-1715.
Stewart, L., K. von Kriegstein, J. D.Warren y T.D. Grifiths (2006), “Music and the brain: Disorders of musical listening’, Brain 129(Pt 10): 2533-2553.
Stuss, D. T. y R. T. Knight (2002), Principles of Frontal Lobe Function. New York: Oxford University Press.
Sutton R. S. y A. G. Barto (1998), Reinforcement Learning: An Introduction. Cambridge, M. A.: MIT Press.
Tervaniemi, et al. (2001), “Superior formation of cortical memory traces for melodic patterns in musicians”, Learn Mem 8(5):295-300.
Thorndike, E. L. (1911), Animal Intelligence. New York: Macmillan.
Tillmann, B. et al. (2006), “Cognitive priming in sung and instrumental music: Activation of inferior frontal cortex”, Neuroimage 31(4): 1771-1782.
Tillmann, B., P. Janata y J. J. Bharucha (2003), “Activation of the inferior frontal cortex in musical priming”, Brain Res Cogn Brain Res 16(2): 145-161.
Trainor, L. J., K. L. McDonald y C. Alain (2002), “Automatic and controlled processing of melodic contour and interval information measured by electrical brain activity”, J Cogn Neurosci 14(3): 430-442.
Vartanian, O. y V. Goel (2004), “Neuroanatomical correlates of aesthetic preference for paintings”, Neuroreport 15(5): 893-897.
Wallin, N., B. Merker y S. Brown (2000), The Origins of Music. Cambridge M. A.: MIT Press.
Wise, R. A. (1978), “Catecholamine theories of reward: A critical review”, Brain Res 152(2): 215-247.
Wright, A. A., J. J. Rivera, S. H. Hulse, M. Shyan y J. J. Neiworth (2000), “Music perception and octave generalization in rhesus monkeys”, J Exp Psychol Gen 129(3):291-307.
Zatorre R. J. y M. Schönwiesner (2011), “Cortical speech and music processes revealed by functional neuroimaging”, The Auditory Cortex. J. A. Winer y C. E. Schreiner /eds.). New York: Springer, pp. 657-677.
Zatorre, R. J., J. L. Chen y V. B. Penhune (2007), “When the brain plays music: Auditory-motor interactions in music perception and production”, Nat Rev Neurosci 8(7): 547-558.
Zatorre, R. J. y A. R. Halpern (2005), “Mental concerts: Musical imagery and auditory cortex”, Neuron 47(1): 9-12.
Zatorre, R. J. (1985), “Discrimination and recognition of tonal melodies after unilateral cerebral excisions”, in Neuropsychologia 23(1): 31-41.
Zatorre, R. J. (1988), “Pitch perception of complex tones and human temporallobe function”, J Acoust Soc Am 84(2): 566-572.
Zatorre, R. J., P. Belin y V. B. Penhune (2002), “Structure and function of auditory cortex: Music and speech”, Trends Cogn Sci 6(1): 37-46.
Zatorre, R. J. y S. R. Baum (2012), “Musical melody and speech intonation: Singing a different tune”, PLoS Biol 10(7): e1001372.
Zatorre, R. J., A. C. Evans y E. Meyer (1994), “Neural mechanisms underlying melodic perception and memory for pitch”, J Neurosci 14(4): 1908-1919.
Zatorre, R. J. y J. T. Gandour (2008), “Neural specializations for speech and pitch: Moving beyond the dichotomies”, Philos Trans R Soc Lond B Biol Sci 363(1493): 1087-1104.

1 comentario en “De La Percepción Al Placer: La Música Y Sus Sustratos Neuronales”
Su sitio es hermoso. Gracias por compartir...